
Isi
- tahap
- Metode 1 Pelajari aturan kelarutan
- Metode 2 Gunakan mnemonik: NAG SAG
- Metode 3 Dasar-dasar pembelajaran
Kelarutan suatu senyawa adalah kemampuannya untuk larut dalam air. Senyawa yang tidak larut akan membentuk endapan dalam larutan. Senyawa terlarut sebagian juga dikatakan tidak larut secara kimia. Jika Anda ingat aturan kelarutan, itu akan membuat hidup Anda lebih mudah ketika Anda harus bekerja dengan persamaan kimia. Dengan sedikit waktu, kerja, dan beberapa trik mnemonik, Anda akan mengingat semua formula.
tahap
Metode 1 Pelajari aturan kelarutan
-

Garam Kelompok 1A larut. Tabel periodik elemen diatur dalam baris dan kolom yang disebut "periode" dan "grup" masing-masing. Kolom pertama tabel berisi elemen-elemen grup 1A. Itu adalah logam alkali. Ini termasuk elemen Li, Na, K, Cs dan Rb.- Contoh: KCl dan LiOH larut dalam air.
-

Garam nitrat, klorat, dan asetat larut. Ketika nitrat (dari rumus NO3), klorat (formula ClO3) atau lacetate (dari rumus CH3COO) membentuk garam, mereka menjadi larut dalam air.- Contoh: KNO3, NaClO3 dan CH3COONa semuanya larut.
-

Semua garam amonium larut. Amonium singa (formula NH4) membentuk garam yang terdisosiasi sepenuhnya dalam air. Tidak ada pengecualian untuk aturan ini.- Contoh: NH4OH larut bahkan jika mengandung ion hidroksida.
-
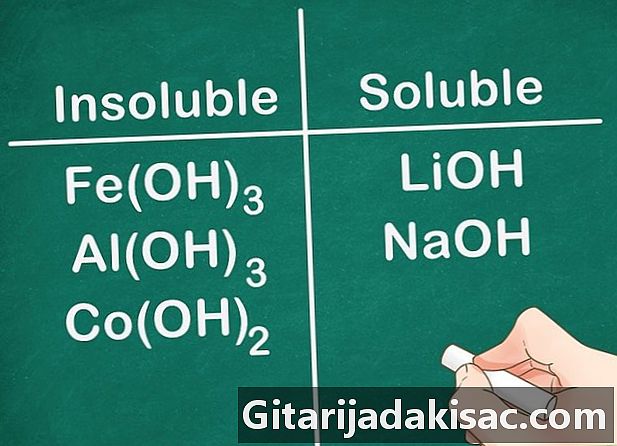
Sebagian besar senyawa hidroksil tidak larut. Beberapa garam hidroksida sedikit larut. Ini adalah kasus hidroksida yang terbentuk dengan unsur-unsur Golongan 2 (Ca, Sr dan Ba). Garam hidroksida yang terbentuk dengan unsur-unsur Golongan 1 merupakan pengecualian karena unsur-unsur ini masih larut.- Contoh: Fe (OH)3, Al (OH)3 dan Co (OH)2 tidak larut, tetapi LiOH dan NaOH larut.
-
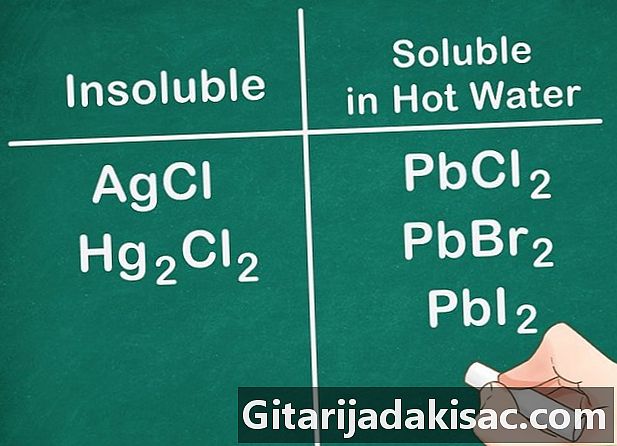
Garam non-logam Golongan 17 umumnya larut. Kelompok 17 bukan logam termasuk klor (Cl), bromida (Br) dan liode (I). Uang, timah, dan merkuri adalah pengecualian dari aturan ini. Senyawa yang terdiri dari bukan logam ini dan ion-ion ini tidak larut.- Contoh: AgCl dan Hg2Cl2 keduanya tidak larut.
- PbCl2, PbBr2 dan PbI2 larut dalam air SANGAT PANAS.
-
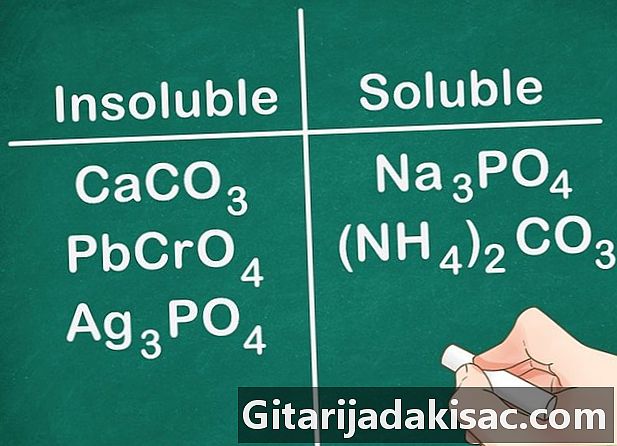
Sebagian besar karbonat, kromat, dan fosfat tidak larut. Formula kimia untuk unsur-unsur ini adalah: CO3 (karbonat), CrO4 (kromat) dan PO4 (Fosfat). Kelompok logam 1A dan senyawa NH4 pengecualian dan larut.- Contoh: senyawa seperti CaCO3, PbCrO4 dan Ag3PO4 semuanya tidak larut sedangkan senyawa seperti Na3PO4 dan (NH4)2CO3 larut.
-
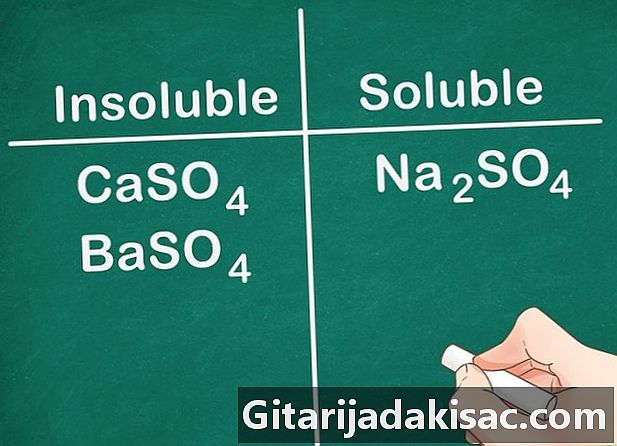
Sebagian besar garam sulfat larut. Sebagian besar garam termasuk ion SO4 larut dalam air. Ca, Ba, Pb, Ag, Sr dan Hg adalah pengecualian dari aturan ini. Garam sulfat yang mengandung ion-ion ini tidak larut.- Contoh: Na2SO4 benar-benar larut sementara CaSO4 dan BaSO4 tidak larut.
-

Sebagian besar senyawa sulfur tidak larut dalam air. Barium, kalsium, magnesium, natrium, kalium, dan amonium adalah pengecualian untuk aturan ini. Hanya senyawa yang terbuat dari unsur-unsur ini dan sulfida yang larut dalam air.- Contoh: CdS, FeS dan ZnS semuanya tidak dapat larut.
- Namun, logam transisi sulfida tidak larut.
Metode 2 Gunakan mnemonik: NAG SAG
-

Gunakan mnemonik NAG SAG mnemonik. Lacronyme NAG SAG adalah trik mudah untuk mengingat senyawa dan pengecualian yang larut. Tulis nama NAG SAG dan hafalkan arti setiap huruf. Teknik ini tidak mengecualikan semua aturan kelarutan, tetapi mencakup sebagian dari mereka. Semua huruf mewakili molekul yang larut.- N: Nitrat (TIDAK3)
- A: Asetat (CH3COO)
- G: Logam alkali grup 1 (Li, Na, dll.)
- S: Sulfat (SO4)
- A: Ion amonium (NH4)
- G: bukan logam dari Grup 17 (F, Cl, Br, I, dll.)
-

Ingat nama PMA untuk pengecualian pertama. P mewakili Pb (timah). M mewakili Merkurius (Hg2). A mewakili Perak (Ag). Ketiga ion ini tidak pernah larut dengan gugus sulfat atau bukan logam dari kelompok 17.- Saat Anda mencatat trik mnemonik, gambar sebuah bintang di dekat akronim PMA dan bintang yang serupa di dekat S dan G dari SAG untuk mengingatkan Anda bahwa itu adalah pengecualian.
-

Ingat kata "Castro" dan "bar" untuk pengecualian kedua. Mungkin terdengar bodoh, tetapi kata-kata ini akan membantu Anda mengingat ion kalsium (Ca, strontium (Sr) dan barium (Ba).) Ketiga ion ini tidak pernah larut dengan sulfat.- Buat tanda silang di sebelah kata-kata ini dan tanda silang lain di dekat S SAG untuk mengingat bahwa ion-ion ini adalah pengecualian untuk kelarutan sulfat.
Metode 3 Dasar-dasar pembelajaran
-

Tinjau sesering mungkin. Mengingat informasi selalu membutuhkan waktu dan kerja. Semakin banyak Anda membaca pelajaran, semakin lama Anda akan mengingatnya. Tinjau peraturan sering dan uji diri Anda sendiri setiap hari pada subjek.- Minta teman atau keluarga untuk bertanya tentang topik ini saat makan siang atau makan malam.
- Simpan salinan aturan untuk ditinjau saat Anda memiliki waktu luang.
-

Buat lembar ringkasan dan gunakan itu. Kartu adalah media yang sangat baik untuk segera merevisi subjek dan menghafalnya. Perhatikan aturan kelarutan pada kartu dengan beberapa contoh. Tinjau lembar sampai Anda terbiasa dengan aturan dan nama senyawa yang larut dan tidak larut.- Bawalah kartu Anda dan bawa keluar untuk diulas di dalam mobil atau sambil menunggu teman-teman Anda.
- Semua peluang bagus untuk meninjau daftar Anda.
-

Gunakan sarana mnemonik. Alat mnemonic adalah tips untuk membantu Anda menghafal informasi dengan cepat dan mudah. Saat Anda mempelajari istilah mnemonik, mungkin berguna untuk menuliskannya beberapa kali untuk mengingatnya. Trik mnemonik hanya berguna jika Anda tahu arti setiap huruf!- Berlatihlah menulis akronim dan apa arti setiap huruf.
- Saat Anda sedang ditinjau, pertama perhatikan tips mnemonic untuk referensi di masa mendatang.